25 Nov 2010 Los materiales de carbono ante los nuevos retos tecnológicos
Rosa Menéndez
Departamento de Química de Materiales, Instituto Nacional del Carbón, (CSIC)
Propiedades y evolución histórica de los materiales de carbono
El carbono, uno de los elementos más abundantes de la naturaleza, tiene la capacidad de combinarse químicamente consigo mismo y con otros elementos mediante fuertes enlaces covalentes dando lugar a una gran variedad de estructuras que permiten el desarrollo de materiales de diversas propiedades [1,2]. Los materiales de carbono pueden ser extremadamente duros como el diamante o fácilmente deslaminables como el grafito; muy densos y con una alta resistencia mecánica (materiales compuestos carbono/carbono), y por consiguiente, adecuados para aplicaciones estructurales (aviones y automóviles de competición), o muy porosos (carbones activados), siendo útiles estos últimos como adsorbentes para almacenamiento de energía o como soporte de catalizadores. Pueden ser altamente conductores (grafito) o aislantes (carbono vítreo). Este amplio espectro de propiedades se ve reforzado por el hecho de que solamente los materiales de carbono son capaces de operar a altas temperaturas en las condiciones más extremas, y por la circunstancia de que no sólo mantienen sus propiedades con la temperatura sino que incluso las mejoran.
Los materiales de carbono han recabado mucha atención con el descubrimiento de los fulerenos y los nanotubos. Sin embargo, los materiales de carbono tradicionales han jugado un importante papel desde los tiempos prehistóricos (pigmento en pinturas rupestres, componente de la pólvora, escritura) y han contribuido al desarrollo industrial y tecnológico de nuestra sociedad (siderurgia).
El descubrimiento de las fibras de carbono, en los años 60, con su elevada resistencia y flexibilidad, supuso un hito importante en el desarrollo de estos materiales. En paralelo, se descubre el carbono vítreo, así denominado por presentar una superficie de fractura concoidal, con unas propiedades similares al vidrio, muy duro y frágil, y con una impermeabilidad a gases no observada hasta entonces en materiales de carbono; sus propiedades son totalmente opuestas a las del grafito. Por las mismas fechas, el hallazgo de nuevas formas estructurales de carbono grafítico, tipo aguja y esferular, contribuyó ostensiblemente al desarrollo de nuevos productos de carbono para muy diversas aplicaciones.
La excelente biocompatibilidad de los materiales de carbono, descubierta en los 70, permitió su utilización en prótesis, ligamentos y válvulas cardíacas, entre otros.
Al inicio de los 80, el desarrollo de la tecnología para la producción de bloques de grafito isótropo de alta densidad permitió su utilización en reactores de alta temperatura, en equipos de síntesis de cristales semiconductores y también para componentes de electrodos de descarga eléctrica. A mediados de los 80, coincide la introducción de las fibras de carbono en ingeniería civil-sistemas arquitectónicos (edificios, puentes) con el descubrimiento de los fulerenos.
En los 90, se descubren los nanotubos, abriendo una nueva era a los materiales de carbono: la era de los nanoestructurados. Ya no se reduce el mundo del carbono a las estructuras planas tipo grafito o tridimensionales tipo diamante, sino que nos encontramos ahora con estructuras cerradas que contienen pentágonos de átomos de C y carbonos tubulares con diámetros en la escala de los nanómetros, constituidos por una lámina sencilla curvada de átomos de carbono en distribución hexagonal. El descubrimiento de los nanotubos de carbono de una sola pared (sencillos) y de pared múltiple estimuló el interés de científicos e ingenieros en campos relacionados con la nanotecnología. Prácticamente en la misma época, surgen nuevas aplicaciones de los materiales de la familia del grafito, tales como materiales anódicos para baterías de ión-Li recargables, fibras de carbono para purificación de agua, electrodos de carbono activado para supercondensadores de doble capa eléctrica, etc.
Ya más recientemente, en 2004, se consiguió aislar por primera vez el grafeno, con una estructura laminar plana, de un átomo de grosor. Sus excepcionales propiedades eléctricas han revolucionado el ámbito científico, encontrando aplicación en electrónica (en ordenadores ultra-rápidos, sustituyendo al silicio), en la futura construcción de ascensores espaciales, en sistemas de protección personal (chalecos antibalas), en el ámbito de la seguridad, etc. En julio de 2008, investigadores de la Universidad de Columbia confirmaron que se trata del material más resistente identificado hasta el momento.
Proceso de formación de los materiales de carbono
El hecho de que los materiales de carbono se puedan obtener a partir de muy diversos precursores y en diferentes medios y condiciones es lo que determina la gran variedad de materiales de carbono existente. Cuando se utiliza un medio líquido o sólido, su estructura depende fundamentalmente de la temperatura utilizada en su preparación y de la composición química del precursor.
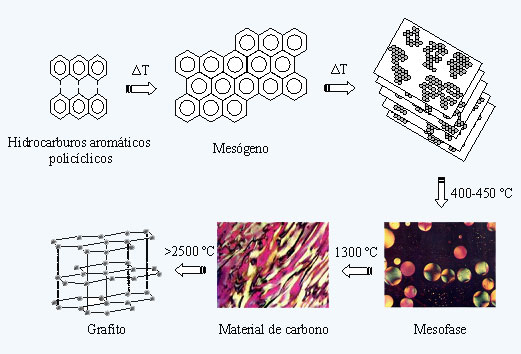
Para obtener materiales en los que el principal componente es el átomo de carbono, los polímeros orgánicos o los hidrocarburos aromáticos policíclicos (puros, mezclas, breas) deben ser tratados térmicamente en atmósfera inerte, proceso que se conoce con el nombre de carbonización. Esta transformación involucra un conjunto de reacciones que van desde la destilación y craqueo térmico de compuestos de bajo peso molecular hasta la polimerización de los componentes más reactivos, que conducen a la formación de un producto sólido carbonoso. En torno a 600 ºC, se eliminan principalmente átomos de oxígeno y nitrógeno en la forma de CO2, CO y (CN)2, junto con CH4. Por encima de 1.000 ºC, se elimina fundamentalmente H2 como consecuencia de la policondensación de los hidrocarburos aromáticos. A partir de 1.300 ºC se obtiene el material de carbono propiamente dicho. Las reacciones que tienen lugar en la transformación de los precursores orgánicos a materiales de carbono inorgánicos (ciclación, aromatización, policondensación) vienen determinadas por el tipo de precursor y las condiciones del tratamiento térmico. Normalmente unos procesos se solapan con otros.
En este proceso de carbonización se forman unidades estructurales básicas, constituidas por asociaciones de moléculas aromáticas planas denominadas mesógenos, que conducen al desarrollo de una fase intermedia tipo cristal líquido que se conoce con el nombre de mesofase (figura 1). La formación de esta fase metaestable durante el proceso de pirólisis está controlada por la topología y tamaño de las moléculas involucradas en el proceso, así como por las condiciones experimentales, y va a ser determinante en la estructura del material de carbono final. Durante el desarrollo de la mesofase, el peso molecular promedio del conjunto continúa incrementándose, y por tanto la viscosidad del sistema, hasta que se alcanza un punto en el que se produce la solidificación. Se pueden obtener materiales que van desde desordenados estructuralmente (isótropos) a altamente ordenados con estructuras tipo grafito, pasando por situaciones intermedias con materiales parcialmente grafitizables con el incremento de la temperatura. La composición química del precursor es un factor clave porque determina la reactividad del sistema durante el proceso de carbonización. De este modo, la presencia de heteroátomos aumenta la reactividad, acelerando el desarrollo de la mesofase, y generando materiales de carbono de bajo orden cristalino con estructuras de pequeño tamaño o incluso totalmente desordenados. Hidrocarburos aromáticos policíclicos, alquil sustituidos y con estructuras nafténicas, favorecen la formación de estructuras ordenadas y cristales de gran tamaño, cuya forma dependerá de las condiciones de procesado. Las propiedades del material final van a venir determinadas por el tamaño y forma de las estructuras cristalinas generadas. El crecimiento de las láminas de carbono y su ordenamiento se consigue a temperaturas por encima de los 2500 ºC, proceso conocido como grafitización. Esta capacidad permite que los materiales de carbono no sólo mantengan sus propiedades mecánicas y de conducción con la temperatura, sino que incluso las mejoren.
Capacidad de diseño de los materiales
Centrándose en la formación de materiales de carbono en medio líquido mediante carbonización de un precursor de carbono, se va a presentar una serie de ejemplos prácticos de la capacidad de manipulación y diseño de materiales a la carta. Se verá como incluso a partir de un mismo precursor orgánico se pueden obtener materiales de muy diversas características por la mera modificación de las condiciones de procesado, o como se pueden mejorar las propiedades de un determinado material.
Los precursores que se utilizan incluyen polímeros termoestables, polímeros termoplásticos, breas y otros derivados del carbón y del petróleo, e hidrocarburos aromáticos policíclicos puros a biomasa. Las variables de procesado sobre las que se puede actuar incluyen temperatura, tiempo de reacción, velocidad de calentamiento, presión, tipo de atmósfera y agitación, entre otras.
La reducción de la velocidad de calentamiento durante el proceso de carbonización de una brea comercial permitió pasar de un material heterogéneo (mezcla de estructuras de distintos tamaños) a otro perfectamente homogéneo, integrado por estructuras de pequeño tamaño que le confieren excelentes propiedades para su utilización en la producción de electrodos para la industria del aluminio [3]. De igual modo, el aumento de presión durante el proceso de carbonización permitió un aumento del tamaño y orientación de las estructuras cristalinas, dando como resultado materiales con una mayor conductividad eléctrica y térmica. No obstante, el efecto más espectacular se observó en el caso de materiales compuestos carbono-carbono, en los que con una brea de impregnación comercial actuando como precursor de la matriz, se obtuvieron materiales con excelentes valores de densidad sin aplicar ciclo de densificación alguno. El factor clave fue el control de la temperatura a la que se aplicó la presión mecánica durante la operación de prensado/moldeo, que coincidió con el punto de fluidez óptimo de la mesofase, y con el tiempo de aplicación [4]. Otro ejemplo práctico de optimización de propiedades de un material lo constituye la aplicación de la estabilización oxidativa a microlaminados de preimpregnados de materiales compuestos, previa al proceso de carbonización. La estabilización oxidativa (tratamiento térmico controlado con aire) del precursor de la matriz evitó la formación de volátiles, y en consecuencia el desarrollo de porosidad en el material. El resultado fue la obtención de un material compuesto unidireccional de elevada densidad [5]. Estos ejemplos ilustran la posibilidad de obtener materiales a partir de precursores comerciales, de bajo coste, sin gravámenes adicionales derivados de la utilización de presión o de sucesivos ciclos de densificación, práctica habitual en aplicaciones como aeronáutica.
Aplicaciones en el campo de la energía
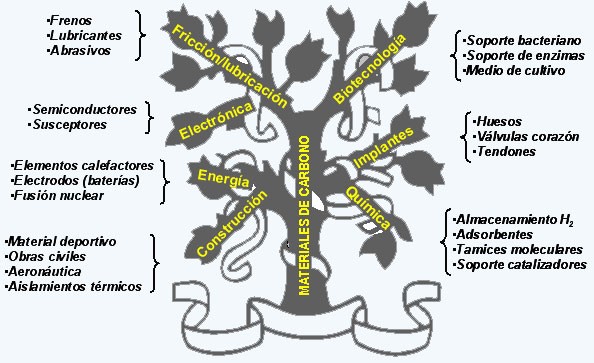
Los materiales de carbono han ampliado su campo de aplicación de forma increíble en los últimos años. Han pasado de un uso tradicional en ánodos para la industria del aluminio, electrodos para la producción de acero, adsorbentes en sistemas de purificación de gases y líquidos (carbones activados) o como componentes de sistemas de frenado de automóviles de competición y militares y aeronáutica, a campos relacionados con el mundo de la energía, el medio ambiente y las comunicaciones. La figura 2 resume el amplio intervalo de aplicaciones en las que se pueden utilizar los materiales de carbono.
Si bien las aplicaciones que se van a ilustrar en este caso se refieren ambas al campo de la energía, los materiales utilizados requieren unas prestaciones completamente diferentes. La primera se relaciona con el diseño de materiales con capacidad para resistir condiciones extremas de operación en reactores de fusión y la segunda con materiales de elevada capacidad de almacenamiento de energía dirigidos al coche eléctrico.
El proyecto ITER (Internacional Termonuclear Experimental Reactor) integra un consorcio internacional (Unión Europea, Japón, Estados Unidos, China, Rusia, Corea del Sur, India) y tiene como objetivo la construcción en Cadarache (Francia) del primer prototipo de reactor de fusión para demostrar la viabilidad científica y tecnológica de la energía nuclear de fusión con fines pacíficos. Está prevista la finalización de su construcción en torno al 2020. La construcción de un segundo dispositivo de demostración de reactor de fusión nuclear (DEMO) para producir y suministrar energía eléctrica está prevista para el 2025, y se espera que entre en operación en torno al 2040. Los materiales de la primera pared de los reactores de fusión (figura 3) son los más directamente expuestos al plasma, y por tanto, a los efectos de las partículas y cargas térmicas que escapan del mismo. Entre los requerimientos de estos materiales están el poseer un alto punto de fusión y una elevada conductividad térmica, de manera que manteniendo su integridad y propiedades, permitan evacuar rápidamente la energía depositada.
Además, deben presentar una elevada resistencia al choque térmico para que no se deterioren ante fenómenos provocados por inestabilidades del plasma. También requieren una elevada resistencia a la erosión química. Los materiales de carbono, concretamente los materiales compuestos carbono-carbono, cumplen con la mayoría de los requerimientos (conductividad térmica, propiedades mecánicas, resistencia a fatiga y choque térmico), sin embargo, las propiedades relacionadas con la resistencia a la erosión química y la retención de tritio deben ser mejoradas. Este ha sido uno de los objetivos del Proyecto Integrado Europeo Extremat, en el que mediante el dopado de la matriz con carburo de titanio se ha conseguido disminuir considerablemente la erosión química y al mismo tiempo mejorar la conductividad térmica en materiales compuestos carbono-carbono 3D [6].
Por otro lado, un problema importante que se plantea en el sector energético para la implantación de las renovables (fotovoltaica y eólica), es la ausencia de sistemas de almacenamiento de energía eficientes que compensen su discontinuidad y la capacidad de respuesta a los picos de demanda. Otro problema asociado a la necesidad de almacenamiento de energía se relaciona con los sistemas móviles, como puede ser la electrónica de consumo o el desarrollo e implantación del vehículo eléctrico. Tres son los dispositivos que ofrecen distintas y complementarias opciones de almacenamiento de energía: las baterías (de ión-Li y flujo red-ox), los supercondensadores y los dispositivos de almacenamiento de hidrógeno para empleo como vector energético en las pilas de combustible. En todos ellos tienen cabida los materiales de carbono.
En el caso de las baterías se han desarrollado nuevos materiales anódicos a partir de residuos del petróleo, de bajo orden estructural, con una capacidad reversible de inserción de Li que supera a la del grafito [7]. En cambio en el caso de los supercondensadores, la estructura y propiedades de los materiales de electrodo son muy diferentes a las de los anteriores. En este caso se requieren materiales con una elevada porosidad y elevada área superficial que les permita generar dispositivos capaces de almacenar grandes densidades de energía [8]. Este es un campo muy prometedor para los materiales de carbono, al poder obtenerse materiales de porosidad controlada y con una química superficial adecuada al tipo de electrolito. Los supercondensadores representan una excelente opción en combinación con las pilas de combustible y las baterías.
En cuanto al empleo de hidrógeno como vector energético para su aplicación en dispositivos móviles (vehículos), su almacenamiento sigue siendo a día de hoy una de las principales limitaciones. La utilización de materiales de carbono de elevada porosidad, y tamaño de poro controlado, se presenta como una de las alternativas más prometedoras.
Nanotubos de carbono, nanofibras y otros materiales de carbono activados compiten en estas aplicaciones. A pesar, de tener el elemento común carbono, sus propiedades y capacidades son muy diferentes, y el factor precio controla inexorablemente los potenciales desarrollos. Cuando se piensa en el coche eléctrico en términos de autonomía se buscan materiales ligeros y capaces de soportar altas presiones, el volumen y la seguridad son clave. Los retos para aumentar la capacidad de adsorción de hidrógeno a bajas temperaturas o elevadas presiones pasan por conseguir aumentar la entalpía de adsorción manteniendo el coste del material. Cuando se piensa en la producción de hidrógeno se plantea una mejora en la dispersión del catalizador, ya que en la actualidad el 90 % es inactivo. Los materiales de carbono por su capacidad de desarrollar porosidad controlada, en combinación con soportes inorgánicos nanoestructurados y metales encapsulados están abriendo nuevas e importantes expectativas de futuro.
Aplicaciones medioambientales
No solamente los gases de efecto invernadero están dañando nuestro ecosistema, sino también otras emisiones locales relacionadas con óxidos de nitrógeno y de azufre procedentes del transporte y de la industria. Los compromisos internacionales adquiridos para paliar sus efectos quedan recogidos en los protocolos de Kyoto (CO2 y otros gases de efecto invernadero), Montreal (emisiones de compuestos de carbono fluorados, capa de ozono) y Sofía (emisiones de óxidos de nitrógeno), así como el convenio LRTAP (emisiones de óxidos de azufre, transporte a larga distancia de contaminantes atmosféricos).
Esta publicación está patrocinada por nuestros socios. Wigs
Los materiales de carbono están siendo ampliamente estudiados y desarrollados para la reducción de emisiones de compuestos orgánicos volátiles y óxidos de nitrógeno en el sector transporte, fundamentalmente en forma de monolitos (estructuras autosoportadas).
Una de las áreas de mayor interés en el campo del tratamiento de aguas residuales y purificación de aguas es el desarrollo de sistemas avanzados de eliminación de contaminantes del agua que mitiguen el impacto medioambiental de los contaminantes eventualmente tóxicos presentes en las mismas. En sistemas de purificación de aguas los materiales de carbono se emplean en procesos de eliminación de contaminantes aromáticos como hidrocarburos policíclicos aromáticos -altamente tóxicos y cancerígenos-, metales pesados (por ejemplo, arsénico, cromo y derivados), eliminación de pesticidas, etc.
Por sus características inherentes, los materiales de carbono son idóneos para su empleo como adsorbente, catalizadores, electrodos o soportes de electrodos. En este campo, es especialmente interesante la utilización de materiales autosoportados (tales como telas de carbono activado, fieltros, o monolitos) como electrodos en procesos electro-asistidos, catálisis y fotocatálisis para promover el tratamiento de aguas residuales a través de la degradación de contaminantes persistentes [8]. Otro campo en el que encuentran una aplicación prometedora es en desalinización de agua, basada en la utilización del material de carbono como electrodo de una celda electroquímica en la que se elimina la sal de la corriente acuosa por efecto de la aplicación de un campo eléctrico.
Para poder materializar y hacer realidad su utilización en el amplio abanico de aplicaciones propuestas y en otras muchas, los materiales de carbono deben superar barreras relacionadas con el desplazamiento de otros materiales tradicionales, en algunos casos, y en otros con la inversión de los fabricantes en nuevos productos, que garantice el suministro de precursores y la producción de los nuevos materiales.
Referencias
(1) Marsh, H. and Rodríguez-Reinoso, F. Science of Carbon Materials. Publicaciones de la Universidad de Alicante, 2000.
(2) Inagaki, M. and Feiyu, K. Tsinghua. Carbon Materials Science and Engineering, University Press, 2006.
(3) Granda, M., Santamaría, R., Menéndez, R., Chemistry and Physics of Carbon, 2003, 28, 263-330.
(4) Casal, E., Bermejo, J., Menéndez, R., Journal of Microscopy, 2001, 201(2), 324-332.
(5) Casal, E., Bermejo, J., Granda, M., Menéndez, R. Journal of Microscopy, 1999, 196(2), 237-242.
(6) Concheso, A. et al, Carbon, 2005, 43, 923-936.
(7) Ruiz, V., Granda, M., Santamaría, R., Blanco, C., Electrochimica Acta, 2009, 54(19), 4481-4486.
(8) Ania, C. O. el al, Water Research, 2007, 41, 333-340